
한국과학기술원(KAIST)은 극단 선택을 한 환자의 뇌 조직을 분석해 우울증의 새로운 분자 기전을 규명했다고 20일 밝혔다.
우울증(MDD)은 세계적으로 흔한 정신질환 가운데 하나지만, 분자적 수준(뇌 속 분자나 단백질, 유전자 수준)에서의 원인은 알려지지 않았다.
우울증 쥐 모델에 스트레스를 유발하자 치아이랑 부위에서 세포 안의 성장·분화 명령을 전달하는 'FGFR1' 수용체가 눈에 띄게 늘어난 모습을 보였다.
특히 FGFR1 유전자를 결손 시킨 녹아웃(Knock-Out·제거) 모델에서 스트레스에 더 취약하고 우울 증상이 빠르게 나타난 모습이 관찰됐다.
이는 FGFR1이 정상적인 신경 조절과 스트레스 저항에 중요한 역할을 함을 의미한다.
연구팀은 광유전학(특정 신경세포에 빛 자극을 줘 선택적으로 제어하는 기법) 기술을 이용, 빛을 통해 FGFR1을 활성화할 수 있는 'optoFGFR1' 시스템을 개발했다.
FGFR1 신호 활성화만으로도 우울 행동을 개선할 수 있음을 실험적으로 입증했다.
하지만 노화된 우울증 쥐 모델에서는 항우울 효과가 나타나지 않았다.
연구팀은 'Numb'라는 단백질이 노화된 뇌에서 과도하게 발현돼 FGFR1의 신호 전달을 방해한다는 사실을 밝혀냈다.
우울증 환자의 사후 뇌 조직에서도 고령의 환자에게서만 Numb 단백질의 특이적 과발현이 나타났다.
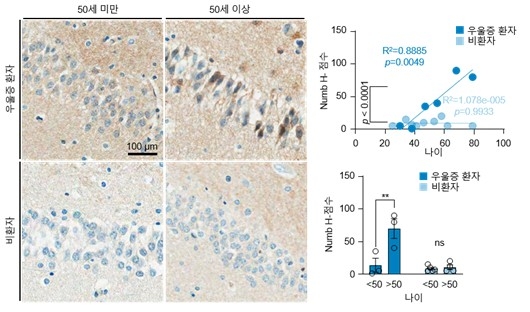
이에 Numb 단백질을 억제하는 유전자를 투여한 결과, 노화 우울증 쥐에게서도 신경 행동이 정상 수준으로 회복된 모습이 나타났다.
허원도 교수는 "우울증이 단순한 신경세포 손상 때문이 아니라 특정 신경신호 경로의 교란에 의해 발생할 수 있음을 밝혔다"며 "고령 환자에게 항우울제가 잘 듣지 않는 이유를 분자적으로 규명하고, Numb 단백질을 표적으로 하는 새로운 치료법 개발에 기여할 것"이라고 말했다.
이번 연구 성과는 국제 학술지 '익스페리멘탈 앤 몰리큘라 메디슨'(Experimental & Molecular Medicine) 지난 15일 자에 실렸다.




