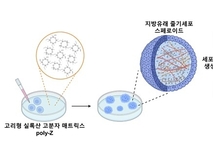
한국과학기술원(KAIST)은 생명과학과 전상용 교수 연구팀이 줄기세포를 더 건강하게 키울 수 있는 새로운 배양 기술을 개발했다고 2일 밝혔다. 연구팀은 세포가 실제 몸속처럼 자랄 수 있도록 돕는 '인공 바닥'(배양 기판)에 고분자 매트릭스(배양 기판 표면을 코팅하는 인공 구조체)를 배열하고, 그 위에서 인간 지방유래 줄기세포(hADSCs)를 입체적으로 배양하는 3차원 플랫폼을 구현했다. 인간 지방유래 줄기세포는 채취가 쉽고 잘 증식하며, 면역 거부 반응이 적어 치료용 세포로 주목받아 왔다. 그러나 기존 2차원(2D·평면) 배양 방식에서는 시간이 지나면서 세포가 늙고 기능이 떨어지는 문제가 있고, 이를 개선하기 위해 세포를 덩어리 형태로 키우는 3차원(3D·입체) 배양 기술이 연구돼 왔음에도 세포가 몸속에서 오래 살아남거나 기능을 유지하는 데는 여전히 한계가 있었다는 게 연구팀의 설명이다. 연구팀은 이런 문제를 해결하기 위해 실록산(실리콘과 산소로 이루어진 생체친화적 고분자 물질)이 촘촘히 가교화된(그물처럼 단단히 연결된 구조) 합성 고분자 물질을 개발하고, 이를 '폴리-지'(poly-Z)로 명명했다. 폴리-지를 기반으로 한 3차원 배양 줄기세포는 다른 세포로

◇ 받은 만큼 돌려준다! 미세순환 순환의 최종 목표인 미세순환은 어떠한 힘으로 일어날까? 혈관 속 물질이 조직세포로 움직이려는 힘은 혈압 때문에 생긴다. 혈관 내 혈압이 주위 세포보다 높기 때문에 물질이 밖으로 빠져나가려는 것이다. 반대로 혈액이 조직세포에서 물질을 받아들일 때는 혈액 속 단백질에 의한 교질삼투압이 작용한다. 이 두 가지 힘의 균형에 의해 물질 이동의 방향이 정해진다. 동맥 쪽 모세혈관에서는 혈액에서 조직세포로, 반대로 정맥 쪽 모세혈관에서는 조직세포에서 혈액으로 움직이려는 힘이 작용하기 때문에 자연스럽게 물질 교환이 일어나게 된다. 그렇다면 조직세포에서는 혈액을 정확히 받은 만큼 돌려줄까? 우리 몸이 아무리 정교하더라도 나간 만큼 들어온다는 게 쉽지는 않다. 혈액이 너무 많이 되돌아오면 수분 부족, 즉 탈수가 일어날 것이고, 반대로 혈액이 너무 적게 돌아오면 수분이 넘쳐 몸이 붓는 부종이 생긴다. 신장 질환이 있는 경우에 부종이 특히 많이 생기기 때문이다. 미세순환 과정에서 오차를 줄여 균형을 유지하는 시스템이 제2의 순환계라 불리는 림프계다. 림프계는 미세순환에서 돌아오지 못한 것을 정맥으로 다시 되돌린다. 림프계는 모세혈관이 존재하는 거

기후변화로 인해 전 세계적으로 대형 산불이 크게 증가하는 가운데 산불 연기(WFS)에 장기간 노출되면 폐암·대장암·유방암·방광암·혈액암 등 발생 위험이 증가할 수 있다는 연구 결과가 나왔다. 미국 뉴멕시코대 종합암센터 치전 우 박사팀은 지난 21일(현지시간) 캘리포니아주 샌디에이고에서 열린 2026년 미국암연구학회(AACR) 연례회의에서 산불 연기 노출과 암 발생 간 연관성을 분석, 이 같은 상관관계를 확인했다고 밝혔다. 우 박사는 "비교적 낮은 수준의 산불 연기 초미세먼지(PM2.5)에서도 암 위험이 증가할 수 있다"며 "중요한 메시지는 산불 연기가 단기적 호흡기·심혈관 문제뿐 아니라 장기적인 암 위험과도 관련될 수 있다는 점"이라고 말했다. 그는 산불 연기에 다환방향족탄화수소(PAH) 같은 발암물질 등 다양한 독성 물질이 포함돼 있다는 것은 알려져 있지만, 실제 환경에서 온몸 건강에 미치는 영향, 특히 암 발생과의 관련성은 여전히 명확하지 않다고 지적했다. 산불 연기 속 독성 화합물은 다양한 생물학적 시스템을 교란하고 초기 노출 부위인 폐뿐 아니라 혈액을 통해 전신으로 퍼질 수 있으며, 연기 노출 자체가 염증 반응을 유발해 발암 과정에도 영향을 미치는 것